Il est réconfortant de penser
qu'on ait récemment, en 1998,
découvert un nouveau
neuromédiateur et d'imaginer qu'il en
reste d'autres à découvrir pour
éclairer les fonctionnements
inexpliqués de notre cerveau. Voir une
mise au point de JG
Sutcliffe et L de Lecea - the hypocretins :
setting the arousal threshold, Nature
Neuroscience vol 3, mai 2002, p339-349. Voir
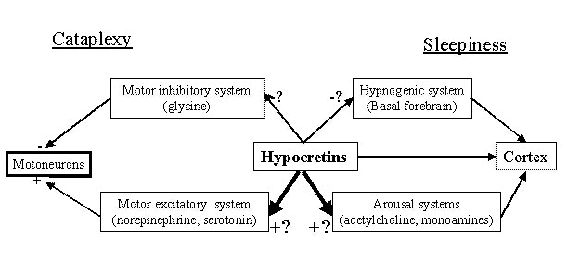
l'illustration : Schematic
model of neurotransmitter circuits that are
involved in the three states of vigilance.
En 1998, deux groupes de chercheurs, sans
lien entre eux, découvrent
simultanément le même neuropeptide,
baptisé "hypocretins" par
de Lecea
L (2) et "orexins" par Sakurai
(12-15). Le plus étonnant reste la
découverte en elle-même, car les
cellules sécrétrices, peu
nombreuses, sont localisées dans une
infime partie de l'hypothalamus latéral.
Les premières observations ont
montré un rôle dans la stimulation
de la satiété, d'où son
appellation orexin (injections dans les
ventricules cérébraux du cerveau
de rats (3,4,6)).
La découverte, en 1999, que la
narcolepsie (1,5) canine était due
à une mutation d'un gêne codant
pour un des récepteurs à
l'hypcretin (Hcrt2), a encouragé
d'étendre les recherches du
contrôle de l'appétit à la
régulation du sommeil. Il apparut
rapidement que l'absence d'hypocrétine
chez la souris avait d'importants effets sur le
comportement et le sommeil rappelant la
narcolepsie ou maladie de Gélineau
(7,10).
D'autres études indiquèrent les
importantes projections des cellules
hypophysaires sécrétrices
d'hypocrétine vers toutes les cellules
monoaminergiques, et l'effet de stimulation de
l'éveil ainsi engendré (3).
Des mesures récentes ont
indiqué que les patients atteints de
narcolepsie avaient des taux effondrés
d'hypocrétine dans le système
nerveux central. A l'heure présente, il
semble que la principale cause de la narcolepsie
soit une destruction par auto-immunité
des cellules hypophysaires
sécrétrices. Les gênes
déterminant l'apparition des
récepteurs à l'hypocrétinee
sont identifiés, ainsi que deux types de
petides actifs sur deux types de
récepteurs (10,11).
La neuroanatomie montre que les cellules
hypothalamiques sécrétrices
projettent sur tout le cortex, le tronc
cérébral, le système
limbique, le thalamus, et vers la moelle
épinière. Des projections denses
et monosynaptiques vers le locus coeruleus (3,8)
indiquent l'importance de ce peptide dans la
régulation de l'éveil. Autre
constat crucial, la répartition des deux
types de récepteurs à
l'hypocrétinee ont des distributions
anatomiques différentes : le locus
coeruleus noradrénergique est
couplé de façon dense avec le type
Hcrt1 et ne contient pas de Hcrt2; le
nucleus tubero-mammillaire histaminergique
contient exclusivement des Hcrt2. L'effet semble
essentiellement excitateur, surtout au niveau du
locus coeruleus, des noyaux du raphé, de
la substantia nigra, des noyaux
tubero-mammillaires (10,11,13)
La différence d'expression de Hctr1 et
Hctr2 peut expliquer le rôle primordial de
Hctr2 dans la narcolepsie. Chez l'animal, la
destruction des récepteurs Hctr2 engendre
un tableau de blocage d'activité motrice
comparabale à la cataplexie et des
accès de sommeil paradoxal. D'autre part,
des animaux porteurs de mutations de Hctr1 ont
des perturbations de leur sommeil lent profond
sans cataplexie (7,10,11,13)
Il n'existe à ce jour aucune
donnée répertoriée
étudiant le bâillement dans la
narcolepsie. La place de l'hypocrétine
dans la neurophysiologie du bâillement
commence à apparaitre
expérimentalement chez le rat :
l'injection d'hypocrétine1 dans le
noyau parventriculaire de l'hypothalamus
déclenche des bâillements en
stimulant la vigilance. L'hypocrétine 2
stimule la vigilance sans déclencher de
bâillements : voir Sato-Suzuki
I, H Arita Cortical arousal induced by
microinjection of orexins into the
paraventricular nucleus of the rat .
L'effet orexigène de
l'hypocrétine, avec un rythme circadien
confirmé, semble jouer un rôle
central dans la régulation
homéostasique de l'apport alimentaire
(2,12). L'obésité est
associée à une réduction
d'activité, un excès de somnolence
mais aucune donnée actuelle ne permet
d'attribuer à un déficit
d'hypocrétine une cause à
certaines obèsités. L'injection
intraventriculaire cérébrale
d'hypocrétine chez l'animal (6),
potentialise la stimulation adrénergique
avec libération de cortisol,
réduction de la prolactine et de
l'hormone de croissance. Chez l'homme la
prolactine et l'hormone de croissance sont au
plus bas pendant le sommeil; le cortisol ne
varie pas au cours de la narcolepsie (7).
En général, les carnivores
bâillent plus que les herbivores, comme
les variations du niveau de leur vigilance le
laissent prédire (Baenninger).
En effet, le rythme de vie des carnivores est
caractérisé par d'importantes
variations du niveau de vigilance, depuis la
tranquilité somnolente, à la
marche, la course après une proie, la
chasse, le dépeçage. Au contraire,
la vie des herbivores est relativement monotone,
et ils passent la plupart de leur temps à
brouter; la difficulté à fabriquer
des protéines à partie de l'herbe
obligent ces mammifères à passer
beaucoup plus de temps de leur éveil
à en ingérer. On peur supposer ici
un rôle régulateur de
l'hypocrétine sur le sommeil et
l'homéostasie énergétique
et donc sur la fréquence des
bâillements.
Les observations de patholologie humaine
montrent le bâillement par excès
comme signe sémiologique d'une
éventuelle pathologie hypophysaire. Par
exemple, l'acromégalie, excès de
fabricaton d'hormone de croissance, se
révèle par des troubles osseux
classiques mais aussi par une asthénie,
une somnolence associée à des
bâillements répétés.
L'adénome hypophysaire peut comprimer les
cellules sécrétrices
d'hypocrétinee, perturber leur
sécrétion; l'augmentation
d'hormone de croissance circulante peut
engendrer un rétrocontrôle
négatif sur la sécrétion de
d'hypocrétinee. Tout reste à
découvrir.
Les très intenses interactions de
l'hypocrétinee avec le système
aminergique tant moléculaire que
cellulaire lui font jouer un rôle dans la
régulation de l'éveil. Comment ne
pas penser que l'hypocrétinee a sa place
dans la neurophysiologie du bâillement
?